Pathologies les plus courantes diagnostiquées avec l’ECG
Bienvenue dans le guide des pathologies les plus fréquentes, diagnostiquées à l’aide de l’ECG. Nous examinerons une série d’affections cardiaques, en étudiant leurs causes et leurs symptômes, et en illustrant la façon dont elles peuvent se manifester sur l’ECG. La détection des stimulateurs cardiaques ou « pacemakers » est également abordée.
Veuillez noter que les pathologies ci-dessous sont présentées en termes simplifiés et illustrées à des fins éducatives uniquement. Le diagnostic ne peut être posé que par un cardiologue.
Dans ce blog, nous abordons les sujets suivants :
Syndromes coronariens aigus
Infarctus du myocarde
Angine de poitrine instable
Péricardite et myocardite
Fibrillation auriculaire
Syndrome de Brugada
Hypertrophie ventriculaire gauche et droite
Hypertrophie ventriculaire gauche
Hypertrophie ventriculaire droite
Tachycardie ventriculaire
Troubles de la conduction
Blocs auriculo-ventriculaires
Blocs de branche gauche et droite
Détection de pacemaker

Apprenez comment réussir un ECG avec un livre électronique complet où nous couvrons:
- Fonctionnement de l’ECG
- Comment effectuer une mesure de l’ECG au repos
- Comment interpréter l’ECG
Pathologies fréquemment diagnostiquées - Interprétation automatique
- Comparaison de différents appareils d’ECG au repos
Syndromes coronariens aigus
Il s’agit d’un groupe de maladies dans lesquelles le flux sanguin vers le cœur diminue. Ces pathologies comprennent l’infarctus du myocarde (STEMI et NSTEMI) et l’angine de poitrine instable.
Infarctus du myocarde
L’infarctus du myocarde (IM), ou familièrement « crise cardiaque », est causé par une diminution ou un arrêt complet de la circulation sanguine dans une partie du myocarde (c’est-à-dire le muscle cardiaque, responsable de la contraction du cœur). Si l’artère coronaire est bloquée, le myocarde ne reçoit pas d’oxygène. Cela peut conduire à la mort et à la nécrose des cellules du myocarde. [3] [4]
L’infarctus du myocarde peut être « silencieux » et passer inaperçu, mais dans le pire des cas, il peut provoquer une détérioration hémodynamique (anomalie du rythme cardiaque et de la pression artérielle) et la mort subite. Les patients peuvent ressentir une gêne thoracique ou une pression irradiant vers le bras, la mâchoire, l’épaule ou le cou.
La présence d’un IM est révélée par des modifications dynamiques sur l’ECG. Même si l’ECG initial ne semble pas pathologique,une surveillance de l’ECG pendant un certain temps peut conduire au diagnostic.
La présence d’un IM est révélée par des modifications dynamiques sur l’ECG. Même si l’ECG initial ne semble pas pathologique,une surveillance de l’ECG pendant un certain temps peut conduire au diagnostic.
Infarctus du myocarde STEMI
Le type STEMI est dû à l’obstruction complète et prolongée d’une ou de plusieurs artères coronaires. Cela provoque une ischémie myocardique transmurale (un manque d’apport sanguin qui affecte toute l’épaisseur du myocarde). Il en résulte une lésion ou une nécrose du myocarde. [5]
Les facteurs de risque des infarctus de type STEMI sont les suivants :
le diabète,
le tabagisme,
la dyslipidémie,
la maladie coronarienne (MC) et
des antécédents familiaux de MC.
Un signe caractéristique est une douleur ou une gêne thoracique, en particulier dans le cas d’un infarctus aigu du myocarde avec élévation du segment ST. Les symptômes sont plus graves que ceux d’un type NSTEMI ou d’un angor instable, car une plus grande partie du myocarde devient ischémique.
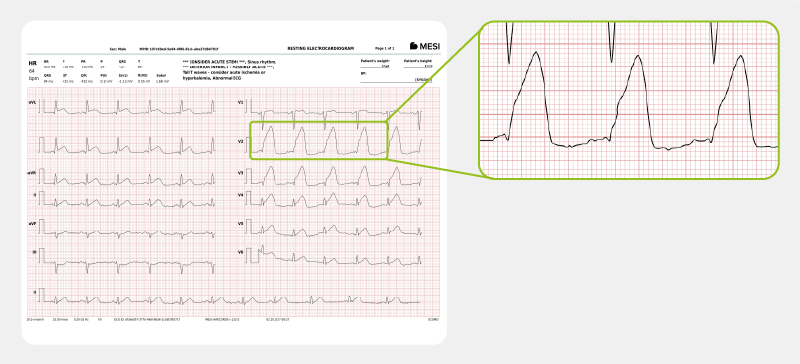
Sur l’ECG, le type STEMI se caractérise par une élévation du segment ST. L’occlusion de l’artère coronaire peut être suivie d’une fibrillation ventriculaire et d’une tachycardie ventriculaire.
Pour un cas réel d’infarctus du myocarde STEMI, cliquez ici.
Infarctus du myocarde NSTEMI
L’infarctus du myocarde NSTEMI est causé par :
un rétrécissement sévère de l’artère coronaire,
une occlusion temporaire, ou
microembolisation of atheroma (fatty
une microembolisation de l’athérome (substance adipeuse présente dans les artères) et/ou
un thrombus (caillot de sang). [5]
Un patient peut être cliniquement instable (par exemple, choc, hypotension, insuffisance ventriculaire gauche). Le signe le plus fréquent est la douleur thoracique, mais elle est moins prononcée que dans l’infarctus du myocarde STEMI, car l’occlusion de l’artère est partielle.
Le type NSTEMI ne présente pas d’élévation du segment ST, mais il y a une élévation des biomarqueurs cardiaques (troponines) comme dans le cas du type STEMI. L’ECG peut révéler des modifications ischémiques, par exemple, des modifications de l’onde T, une dépression du segment ST ou une élévation transitoire du segment ST ; cependant, il peut également montrer des modifications non spécifiques ou être normal.
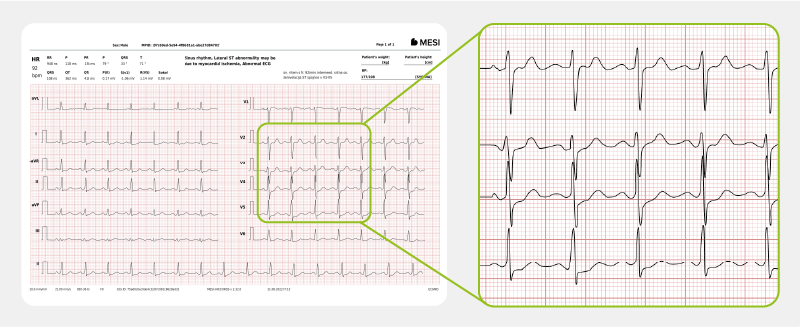
Pour un cas réel d’infarctus du myocarde NSTEMI, cliquez ici.
Angine de poitrine instable
L’angine de poitrine instable est une gêne ou une douleur thoracique causée par un flux insuffisant de sang et d’oxygène vers le cœur. Elle peut entraîner un infarctus du myocarde. [6]
Cette affection est causée par la maladie athérosclérotique coronarienne –une accumulation de plaque dans les artères coronaires conduisant à un thrombus qui bloque partiellement le flux sanguin. Plus rarement, elle est causée par un vasospasme d’une artère coronaire.
Les facteurs de risque sont les suivants :
le diabète,
l’hypertension,
les antécédents familiaux,
l’obésité,
l’insuffisance rénale chronique,
l’anémie,
les troubles auto-immuns,
le tabagisme (actuel ou passé) et
l’abus de substances (cocaïne, amphétamines).
À la différence de l’infarctus, l’angine de poitrine instable présente des taux de troponine normaux.
Les symptômes sont les mêmes que ceux de la maladie coronarienne athérosclérotique. Le symptôme le plus fréquent est l’essoufflement et la douleur thoracique. En revanche, il est plus faible que dans l’infarctus du myocarde STEMI à cause de l’occlusion partielle de l’artère coronaire. Cette douleur ou cette gêne peut irradier vers l’un des bras ou la mâchoire. Des vomissements, des nausées, des vertiges, des diaphorèses et des palpitations peuvent également survenir. La douleur peut s’aggraver avec l’effort physique et diminuer avec le repos.
L’ECG de l’angor instable peut montrer des ondes T aplaties, des ondes T suraiguës, des ondes T inversées et une dépression ST. Les élévations du segment ST indiquent un infarctus STEMI. Le rythme sinusal est différent de celui d’un infarctus.
Péricardite et myocardite
Ces deux affections sont des inflammations dans différentes parties du cœur. Elles sont difficiles à distinguer, car elles sont souvent présentes ensemble.
Péricardite
Il s’agit d’une inflammation du péricarde (le sac qui contient le cœur et les racines des principaux vaisseaux). Le plus souvent, la péricardite est causée par une infection (virale) etelle peut donc affecter des patients de tous âges.
Elle peut également avoir de nombreuses causes systémiques et locales :
après l’infarctus,
infarctus aigu du myocarde,
polyarthrite rhumatoïde,
lupus,
tuberculose,
post-chirurgie cardiaque (péricardite hémorragique), etc.
Le symptôme le plus fréquent de la péricardite est la douleur thoracique, difficile à différencier de l’infarctus aigu. La douleur peut être forte et accompagnée de sueurs froides, d’anxiété et/ou de tachycardie.
Myocardite
Inflammation du myocarde et de l’interstitium (l’espace conjonctif entre les cellules du tissu myocardique).
Elle peu être causée par :
une infection virale ou bactérienne,
des réactions auto-immunes,
des champignons,
des parasites,
une borréliose et
le VIH/SIDA.
Les patients présentent un rythme cardiaque anormal, une faible douleur thoracique et une insuffisance cardiaque progressive.
Sur l’ECG, la péricardite aiguë et la myocardite sont caractérisées par des modifications non spécifiques du segment ST. Il peut également y avoir des irrégularités dans le rythme ventriculaire et supraventriculaire, ainsi que des anomalies de l’onde T.
Fibrillation auriculaire
La fibrillation auriculaire est la tachyarythmie pathologique la plus courante (rythme cardiaque anormal avec une fréquence cardiaque de plus de 100 battements par minute). L’affection se produit soudainement dans les oreillettes du cœur.
Les signes ECG courants de la fibrillation auriculaire sont une fréquence ventriculaire irrégulière et l’absence d’ondes P.
Les symptômes les plus courants sont (une combinaison de) fatigue, gêne dans la gorge et la poitrine, palpitations, dyspnée et diminution de la capacité à faire de l’exercice. Environ un quart despatients ne présentent pas de symptômes ; dansce cas, la maladie est détectéeau moyen de l’ECG.
Le risque de cette pathologie augmente avec l’âge. Elle survient chez moins de 1 % des personnes âgées de 60 à 65 ans, mais chez 8 à 10 % des personnes âgées de plus de 80 ans.
Le risque est également accru par :
l’hypertension,
les troubles respiratoires liés au sommeil,
les valvulopathies et
l’insuffisance cardiaque congestive.
Les signes ECG courants de la fibrillation auriculaire sont une fréquence ventriculaire irrégulière et l’absence d’ondes P.

Syndrome de Brugada
Le syndrome de Brugada (BrS) est une arythmie héréditaire rare. Il peut entraîner une fibrillation ventriculaire potentiellement mortelle et une mort cardiaque subite, sans anomalie structurelle identifiable. [8]
Cette maladie touche généralement des patients d’âge moyen (45 ans au moment du diagnostic), avec une incidence huit fois plus élevée chez les hommes.
Les facteurs de risque du syndrome de Brugada sont les suivants :
des antécédents familiaux de cette maladie,
l’origine raciale (plus fréquente chez les personnes d’origine asiatique),
la fièvre (elle ne provoque pas l’affection, mais elle peut irriter le cœur, et donc être un facteur déclenchant), et
la consommation de certains médicaments sur ordonnance ou de cocaïne.
De nombreux patients atteints de BrS sont asymptomatiques. La syncope (évanouissement dû à un flux sanguin anormal dans le cerveau) ou la mort cardiaque subite (avortée) sont souvent les premiers symptômes. Ils apparaissent fréquemmentla nuit ou au repos.
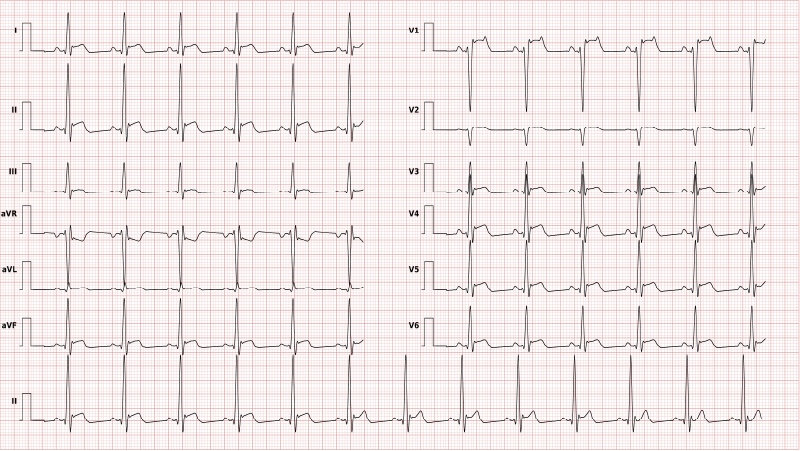
L’ECG montre un schéma spécifique, mais labile, défini par une élévation ≥ 0,2 mV du segment STdans les dérivations précordiales(V1-V3). L’ECG peut également être « silencieux »(non spécifique) et des bloqueurs de sodium sontappliqués pour que l’affection se manifeste.

Hypertrophie ventriculaire gauche et droite
Dans l’hypertrophie, le muscle cardiaque devient plus épais pour diverses raisons. L’ECG permet de distinguer l’hypertrophie ventriculaire gauche de l’hypertrophie ventriculaire droite. [9] [10]
Hypertrophie ventriculaire gauche
L’hypertrophie ventriculaire gauche (HVG) est due à une augmentation de la charge de travail du ventricule gauche, par exemple, en raison d’une sténose de la valve aortique ou d’une hypertension.
L’hypertrophie ventriculaire gauche peut être présente sans symptômes pendant des années. Au fur et à mesure qu’elle s’aggrave, la fatigue, l’essoufflement, les palpitations cardiaques, les douleurs thoraciques (surtout pendant l’exercice), les vertiges ou l’évanouissement peuvent apparaître.
Due to the left ventricular wall thickening, the QRS complexes become larger, especially in leads V1-V6. There is a deep S wave in V1 and a high R wave in V4. Some ST depression is often observed in leads V5-V6 (so-called ‘strain pattern’).
L’hypertrophie ventriculaire gauche peut être présente sans symptômes pendant des années. Au fur et à mesure qu’elle s’aggrave, la fatigue, l’essoufflement, les palpitations cardiaques, les douleurs thoraciques (surtout pendant l’exercice), les vertiges ou l’évanouissement peuvent apparaître.

Hypertrophie ventriculaire droite
L’hypertrophie ventriculaire droite (HVD) est due à une augmentation de la charge de travail du ventricule droit, par exemple, en raison d’une embolie pulmonaire ou d’un emphysème.
L’HVD est due à une cardiopathie congénitale ou à une maladie pulmonaire. L’affection elle-même peut ne présenter aucun symptôme, mais il peut y en avoir en raison des problèmes cardiaques ou pulmonaires associés.
L’ECG montre un complexe QRS négatif en I (et donc un axe cardiaque droit) ainsi qu’un complexe QRS positif en V1.

Tachycardie ventriculaire
La tachycardie ventriculaire (TV) est un trouble du rythme (arythmie) potentiellement mortel dans les ventricules cardiaques. [11]
Les manifestations cliniques et les conséquences de la TV sont diverses :
la fibrillation ventriculaire,
la syncope,
un orage électrique,
un choc cardiogénique,
un arrêt cardiaque et
la mort cardiaque subite.
La TV survient fréquemment à cause des facteurs suivants :
les maladies cardiaques structurelles (maladies qui affectent les muscles, les cavités, les parois ou les valves du cœur),
les canalopathies (c’est-à-dire le syndrome de Brugada),
l’ischémie,
des troubles électrolytiques, et
autour de tissus cicatriciels anciens dans le cœur, par exemple, après un infarctus du myocarde.
La TV est une séquence de trois battements ventriculaires ou plus, dont la fréquence est supérieure à 100 bpm, le plus souvent entre 110 et 250 bpm. Les défibrillateurs cardioverteurs implantables (DCI) constituent la principale stratégie de prise en charge de la TV. Ils réduisent le nombre de décès, mais pas les récidives de TV.
La TV est une séquence de trois battements ventriculaires ou plus, dont la fréquence est supérieure à 100 bpm, le plus souvent entre 110 et 250 bpm. Les défibrillateurs cardioverteurs implantables (DCI) constituent la principale stratégie de prise en charge de la TV. Ils réduisent le nombre de décès, mais pas les récidives de TV.

Troubles de la conduction
Les troubles de la conduction ou blocs cardiaques sont des problèmes du système de conduction cardiaque, qui contrôle la fréquence et le rythme cardiaques.
Blocs auriculo-ventriculaires
La conduction entre les oreillettes et les ventricules est perturbée. [12]
En fonction de la gravité, les symptômes suivants peuvent apparaître :
douleur thoracique,
fatigue,
dyspnée,
(pré)syncope,
arrêt cardiaque soudain.
Les blocs auriculo-ventriculaires entraînent une augmentation de l’intervalle PQ ou des ondes P (c’est-à-dire une activité auriculaire) qui ne sont pas (immédiatement) suivies par des complexes QRS (c’est-à-dire une activité ventriculaire). Ceci est clairement visible surl’ECG.
Il existe trois degrés de bloc auriculo-ventriculaire. Ils diffèrent par leur gravité.
BLOC AV DU PREMIER DEGRÉ
Ce degré est relativement inoffensif car le complexe QRS est tardif, mais pas absent. Certaines personnes naissent avec cette condition et peuvent mener une vie normale si elle ne s’aggrave pas. Autres causes :
l’infarctus du myocarde inférieur,
la myocardite,
une augmentation du tonus vagal (par exemple, chez les athlètes),
hyperkaliémie,
la post-chirurgie cardiaque et les médicaments (par exemple, bêta-bloquants), et
l’âge avancé en raison de la dégénérescence du système de conduction.
Le bloc AV du premier degré se caractérise par un PQ prolongé (> 0,20 seconde), suivi du complexe QRS.

BLOC AV DU DEUXIÈME DEGRÉ MOBITZ TYPE 2
Les battements du cœur sont irréguliers. Une instabilité hémodynamique ou une bradycardie peut survenir à tout moment, entraînant une syncope ou même une mort cardiaque subite. Un stimulateur cardiaque (pacemaker) est nécessaire.
Voici quelques-unes des causes :
un infarctus antérieur entraînant un infarctus et une nécrose septale ;
une fibrose idiopathique du système de conduction ;
des inflammations (par exemple, maladie de Lyme, myocardite) ;
autoimmune conditions (e.g. lupus, sclerosis);
des maladies auto-immunes (par ex., le lupus, la sclérose) ;
le déséquilibre électrolytique (par ex., hyperkaliémie) ;
après une chirurgie cardiaque (par ex., réparation de la valve mitrale) ;
des médicaments (par ex., inhibiteurs calciques non dihydropyridiniques, bêta-bloquants).
Il n’y a pas d’allongement du QP dans le bloc AV de Mobitz de type 2. Il existe un risque d’aggravation vers un bloc cardiaque complet.

BLOC AV DU TROISIÈME DEGRÉ
Le bloc est total – il n’y a aucune conduction auriculo-ventriculaire. L’apport sanguin au cerveau peut être insuffisant, ce qui entraîne une perte de conscience.
L’absence de rythme ventriculaire entraîne l’asystolie et la mort. Les causes sont souvent les mêmes que pour le bloc AV du second degré, y compris la dégénérescence du système de conduction due à l’âge avancé.
Un stimulateur cardiaque (pacemaker) permanent est nécessaire.
Sur l’ECG, il n’y a pas de lien entre les ondes P et les complexes QRS .

Blocs de branche gauche et droite
BLOC DE BRANCHE GAUCHE (BBG)
En cas de BBG, la conduction dans le faisceau gauche est lente. [13] [14]
Certains facteurs sont :
l’hypertension,
la myocardite,
l’hypertrophie ventriculaire,
la cardiopathie ischémique et
l’insuffisance cardiaque.
Les principales causes sont l’ischémie et l’infarctus ; le BBG peut également les imiter ou les masquer. Par conséquent, la prise en charge du BBG est similaire à celle de l’infarctus aigu du myocarde avec élévation du segment ST.
Le BBG est asymptomatique, mais il existe un schéma ECG caractéristique. La conduction est lente, ce qui entraîne une dépolarisation retardée du ventricule gauche. En raison d’une dépolarisation plus lente du ventricule gauche, on observe un QRS négatif important dans V1-V3.

BLOC DE BRANCHE DROIT (BBD)
La conduction dans le faisceau droit est lente. Il peut y avoir un retard ou une obstruction partielle sur le chemin des impulsions électriques vers le ventricule droit (« BBD incomplet ») ou une obstruction complète (« BBD complet »).
Certaines personnes naissent avec un BBD incomplet et peuvent mener une vie normale. Elle est également causée par d’autres conditions telles que :
l’hypertension,
les troubles cardiaques structurels (par exemple, myocardite, cardiomyopathie, cardiopathie ischémique),
le syndrome de Brugada ou
l’hypertension pulmonaire.
Le BBD est le plus souvent asymptomatique et est souvent détecté accidentellement lors d’un ECG de routine. Occasionnellement, un évanouissement (présyncope) peut se produire et doit être examiné, car des blocages graves peuvent s’ensuivre.
La dépolarisation du ventricule droit est retardée, de sorte que l’activité électrique du ventricule gauche est pratiquement terminée à ce moment-là. La dernière activité électrique est donc visible à droite, avec un complexe QRS nettement positif dans V1.

Détection de pacemaker
Un stimulateur cardiaque, ou pacemaker, est implanté lorsque la conduction des impulsions électriques dans le cœur est dangereusement perturbée en raison de rythmes cardiaques anormaux qui font que le cœur manque des pulsations ou bat trop lentement. [16]
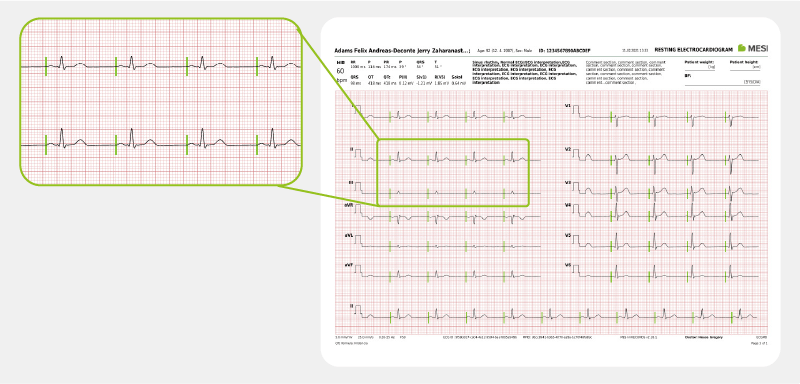
Le rythme du stimulateur cardiaque peut être détecté sur l’ECG. Il est représenté par des pointes de pacemaker – des signaux verticaux qui représentent l’activité de stimulation électrique du pacemaker.